电沉积法制备CuInS2薄膜
本文采用单步电沉积法和两步电沉积法在Mo基底上制备CuInS2薄膜,用X射线衍射仪(XRD)和扫描电子显微镜(SEM)表征了样品的结构和形貌,用能量散射仪(EDX)测试了样品中各元素含量。结果表明,电沉积法制备的样品,元素原子比与沉积电位密切相关;单步法制备的薄膜样品,致密平整,晶粒大小1~2 μm,CuInS2晶体呈黄铜矿结构,同时含有CuS晶体;两步法制备的CuInS2薄膜为黄铜矿结构,无杂相,但薄膜的致密平整性不如单步法。
CuInS2是I–III–VI2族直接能隙半导体化合物,禁带宽度1.50 eV,对可见光的吸收系数高达105 cm-1数量级,以其作为太阳电池的光吸收层,厚度仅需l~2 μm,可极大地降低成本。据Meese J M等的理论计算,CuInS2薄膜太阳电池的光电转换效率理论值超过30%,实验室水平已达到12.5%,而且其抗干扰、抗辐射能力强,性能稳定,制成的光伏器件使用寿命长。因此,CuInS2是薄膜太阳电池光吸收层最有前途的材料之一。
目前CuInS2薄膜的制备大致可以分为直接合成法和多步硫化法两种。直接合成法包括单源、双源或三源共蒸发法,原子层沉积法,离子层气相反应法,电化学法,喷雾热解法等,多步硫化法则须先用蒸发、溅射或电化学沉积等方法制备金属预置层,然后再对其进行硫化来制备CuInS2薄膜。但是上述的大多数方法都必须在高真空条件下进行,对实验条件和实验设备的要求苛刻,不利于低成本大规模生产。用电沉积法制备CuInS2薄膜则无需高真空条件,同时其具有可实现大面积制备、能源消耗少、成本低、系统稳定性好等优点。电沉积法制备CuInS2薄膜有单步法、两步法和多步法。目前对电沉积法制备CuInS2薄膜的研究较少,制备工艺也不成熟。单步电沉积法和两步电沉积法各有优劣,本文研究不同沉积电位对电沉积法制备CuInS2薄膜的影响,对比研究单步法和两步法制备CuInS2薄膜,探索电沉积法制备CuInS2薄膜的最佳工艺。
1、实验
电沉积法制备CuInS2薄膜的电解池采用三电极体系,其中Mo 片(25mm×20mm×0.15mm)为工作电极,Pt电极为辅助电极,饱和甘汞电极(SCE)为参比电极,Mo 片经打磨-去离子水洗-20%wt 的NaOH 溶液煮沸清洗-电化学抛光处理。单步电沉积中电解液为10 mmol/L CuCl2,10mmol/L InCl3,50 mmol/L Na2S2O3 和200 mmol/LLiCl 的混合液,用稀盐酸调节电解液pH 至3.0。其中,CuCl2、InCl3、Na2S2O3 分别作为Cu 源、In 源和S 源,LiCl 既有络合剂的作用,又是合适的添加剂。电沉积过程采用恒压模式,保持工作电极与参比电极间的电压VSCE 恒定,常温下沉积,时间为30 min,沉积后的样品在低真空条件下350 oC 热处理60 min。两步电沉积法制备CuInS2 薄膜,电解液为10 mmol/L CuCl2,10 mmol/L InCl3 和200 mmol/L LiCl 的混合液,用稀盐酸调节电解液pH至2.5。沉积电位为-1.1 V vs.SCE,常温下沉积30 min,沉积后的样品在硫气氛中热处理,250℃和500℃温度下分别处理30 min。
用X射线衍射仪(Rigaku D/MAX-RB,Cu Kα λ=1.54056 Å/40 kV/60 mA)表征样品的晶体结构,用扫描电子显微镜(SEM,JEOL JSM-6390)观察样品的微观形貌,用能量散射仪(EDX,Bruker AXS Microanalysis Esprit 1.8)测试样品中各元素含量。
2、实验结果
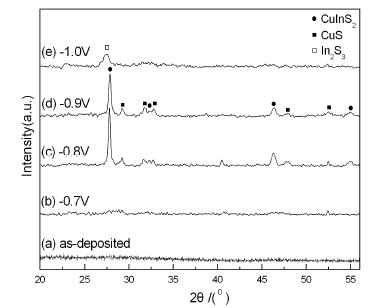
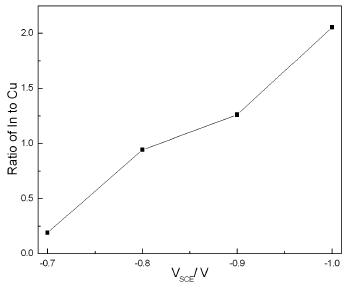

图1 单步电沉积法不同沉积电位下薄膜的XRD 图 图2 单步电沉积法不同沉积电位下薄膜的In/Cu 原子比 图3 单步电沉积法不同沉积电位下制备薄膜的SEM 图
图1为恒定反应物浓度、溶液pH值、沉积时间及热处理温度,改变沉积电位从-0.7 V到-1.0 V变化,用单步电沉积法制备的薄膜的XRD图。
图2为不同沉积电位时薄膜中In/Cu原子比。随着沉积电位的增加,In/Cu原子比呈线性增加。沉积电位为-0.8 V和-0.9 V时,In/Cu原子比均在1.0附近,而其他沉积电位下,In/Cu原子比偏离1.0很大,尤其在低电位情况下,In元素析出量远小于Cu。 实验采用的电化学体系以饱和甘汞电极为参比电极,改变工作电极相对于参比电极的电压VSCE,就改变了工作电极内电子的能量。电解液与工作电极之间发生电子流动的临界电势与电解液中对应的化学物质的标准电势有关。实验中,电解池内发生反应的化学物质的标准电势如式(1)~(3)所示:
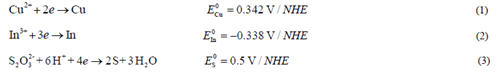
由能斯特方程推导出析出电位表达式如式(4)所示:
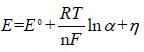 (4)
(4)
其中E0为相对标准氢电极电位,n 为参加反应的离子带电荷数,F为法拉第常数,η为金属离子在阴极上放电的过电位,由电极过程动力学因素以及有关参数决定,α 为金属离子的平均活度。
由式(1),(2)可知Cu 和In 两者的标准电势相差很大,而析出电位越正的金属离子越容易析出。Cu 元素的标准电势远高于In 元素,当沉积电位较低时,Cu 的析出电位高于In,Cu 元素更易析出,沉积样品中Cu 元素含量远高于In。增大沉积电位,可提高阴极极化强度,由式(4)可知,析出电位会随之增加,减小不同元素析出电位的差距。随着沉积电位增加,In/Cu 原子比增大。复合电沉积中,元素共沉积的条件是不同离子的析出电位相近。为得到理想配比的Cu、In 比例,调节沉积电压以改变阴极的极化强度,使不同元素的析出电位接近。本实验中,沉积电位为-0.8 V 和-0.9 V 时,Cu 元素和In 元素的原子比接近1.0,在该电位下沉积,能够得到符合化学计量比的CuInS2 薄膜,图1 所示的XRD 图也能说明此点。