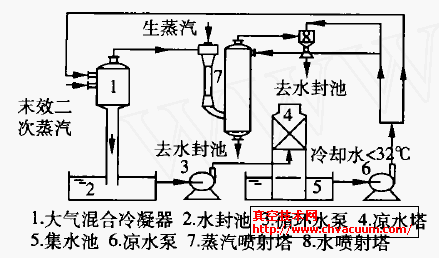
碘盐中碘酸钾与其它形态碘的分离
近年来对被称为“智力元素”的碘的研究越来越广泛。加碘盐是最经济简便的补碘方法,人们在研究食用加碘盐中碘的损失原因的同时,不得不对碘在碘盐中存在的形态的研究也越来越深入。作者发现碘在碘盐中比较普遍及稳定的存在形态是碘酸盐与碘化物。并找到了一种分离剂将其分离后,采用次氯酸钠氧化-还原法分别测定, 从而确定不同形态存在的碘的量。
1、实验部分
1.1、范围
本方法适用于加碘盐中碘酸盐与碘化物的分别测定。
1.2、原理:样品经无水酒精分离为碘酸盐和碘化物两部分,分别在酸性溶液中,次氯酸钠将碘氧化成碘酸根,草酸除去过剩的次氯酸钠,碘酸根氧化碘化钾析出碘,用硫代硫酸钠标准溶液滴定,分别测定碘离子的含量。反应方程式为:
3CIO- +I- →IO3-+3CI-
H2C2O4+CIO- →CI- +2CO2+H2O
IO3- +5I- +6H+ →3I2+3H2O
2S2O3 2- +I2→2I - +S4O6 2-
1.3、仪器及试剂
1.3.1、磁力搅拌器
1.3.2、分离剂:无水酒精(AR)
1.3.3、草酸-磷酸混合液:称取15g 草酸,加水溶解,加入85%磷酸34mL,加水稀释到500mL;
1.3.4、次氯酸钠:5%的溶液;
1.3.5、碘化钾:50g/L;
1.3.6、淀粉:5g/L;
1.3.7、硫代硫酸钠标准溶液:0.002000mol/L。
1.4、实验方法
定量称取研磨后的样品于小烧杯中,加入分离剂,于搅拌器上搅拌洗涤,过滤,漏干,重复以上操作过程,将滤纸上及烧杯中剩样转入碘量瓶中(滤液转入另一碘量瓶中,蒸干,同下操作),加水80mL、2.0mL 草酸-磷酸混合液,用水洗净瓶壁,加热溶解样品,至刚刚沸腾时立即取下,冷至35℃以下,加入5mL 碘化钾溶液,用硫代硫酸钠标准溶液滴定。滴定到溶液呈浅黄色时,加入5mL 淀粉溶液,继续滴定至蓝色恰好消失为止。
2、结果与讨论
2.1、分离剂的用量
在试验过程中我们加入10、20、30、40、50mL不等量的分离剂进行分离,结果显示如图1可知,随着分离剂加入量的增加,分离率呈递增趋势,但在加入量为20mL 后洗涤效果基本稳定,故确定加入分离剂量为20mL。

2.2、洗涤所用的时间
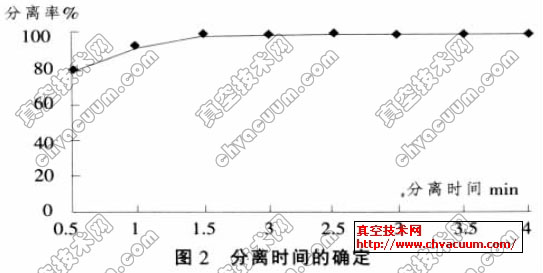
在确定洗涤所用的时间主要以分离剂充分溶解盐样中的碘化物为准,作者在0.5~4min内进行试验,试验显示如图2,由图可看出,随着洗涤搅拌时间的增加,分离率越来越高,在洗涤时间1.5min后,分离效果已趋稳定,所以我们选择2min。
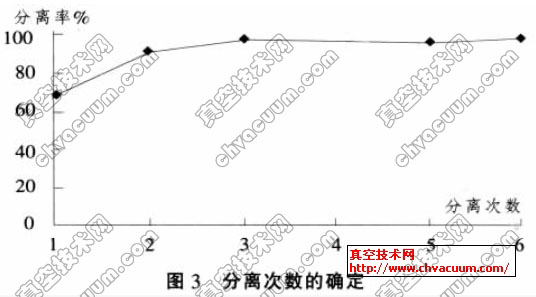
2.3、分离次数的确定
我们分别对样品进行从1-6次的分离,分离结果显示如图3,由图可知,样品分离次数越多,分离率也越高,且在分离3次后分率后呈稳定状态,故选用4 次。
2.4、精密度
本法测定6次碘盐中碘酸盐的相对标准偏差为1.14%; 测定6次碘盐中以其它形态存在的碘的相对偏差为1.20%。
注:本试验结果均以碘计。
2.5、加标回收率实验
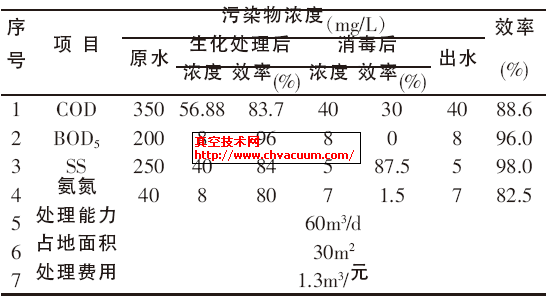
对本法进行回收率实验,以30mg/kg的碘酸钾加入(以碘计),6次的平均回收率为98.16%;以30mg/kg的碘化钾加入(以碘计),6次的平均回收率为97.6%。结果见表1。
表1 样品测定结果(n=6)

3、操作注意事项
3.1、样品将碘酸盐与其它形态的碘进行分离后,可用本文中前边提到的次氯酸钠氧化-还原法分别测定,也可用溴水氧化法分别测定碘的含量,从而确定不同形态存在的碘的量。
3.2、本方法在样品测定时收集到的滤液进行其它形态的碘测定时,要将分离剂蒸发至干。如果在氧化法还原法测定碘时含有乙醇量达到一定量时,在滴定终点加入淀粉时就会形成混浊液,无法对样品测定。
4、结论
本文详细阐述了碘盐中碘酸钾与以其它形态的碘的分离过程以及其含量的分别测定。前处理简单,便于操作。方法延承了氧化还原法测定碘的各种优点,回收率高、定量检测限很低等,精密度和准确度均能满足分析测定要求。